Химични и физични свойства на алуминия. Физични свойства на алуминиев хидроксид
Този лек метал със сребристо-бял нюанс се среща почти навсякъде в съвременния живот. Физическите и химичните свойства на алуминия го използват широко в промишлеността. Най-известните находища са в Африка, Южна Америка и Карибите. В Русия местата за добив на боксит се намират в Урал. Световни лидери в производството на алуминий са Китай, Русия, Канада, САЩ. 
Ал мин
В природата този сребърен метал, поради високата си химическа активност, се намира само под формата на съединения. Най-известните геоложки скали, съдържащи алуминий, са боксит, двуалуминиев триоксид, корунд, фелдшпатите. Бокситите и двуалуминиевият триоксид са от промишлено значение, именно отлаганията на тези руди позволяват извличането на алуминий в чист вид.
свойства
Физическите свойства на алуминия улесняват издърпването на заготовката от този метал в тел и се навива на тънки листове. Този метал не е траен, за да се увеличи този показател по време на топенето, той се легира с различни добавки: мед, силиций, магнезий, манган, цинк. За промишлени цели е важно друго физическо свойство на алуминиева субстанция да бъде неговата способност да окислява бързо във въздуха. В естествени условия повърхността на алуминиевия продукт обикновено се покрива с тънък оксиден филм, който ефективно предпазва метала и предотвратява корозията му. Когато този филм се разруши, сребристият метал бързо се окислява, докато температурата се повишава значително.
Вътрешната структура на алуминия
Физическите и химичните свойства на алуминия до голяма степен зависят от неговата вътрешна структура. Кристална решетка Този елемент е тип лицево-центриран куб. 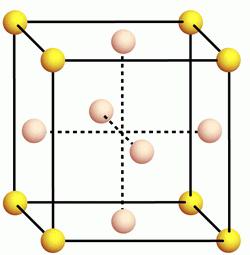 Този вид решетка е присъща на много метали, като мед, бром, сребро, злато, кобалт и други. Високата топлопроводимост и способността за провеждане на електричество направиха този метал един от най-търсените в света. Останалите физични свойства на алуминия, чиято таблица е представена по-долу, напълно разкриват неговите свойства и показват обхвата на тяхното приложение.
Този вид решетка е присъща на много метали, като мед, бром, сребро, злато, кобалт и други. Високата топлопроводимост и способността за провеждане на електричество направиха този метал един от най-търсените в света. Останалите физични свойства на алуминия, чиято таблица е представена по-долу, напълно разкриват неговите свойства и показват обхвата на тяхното приложение. 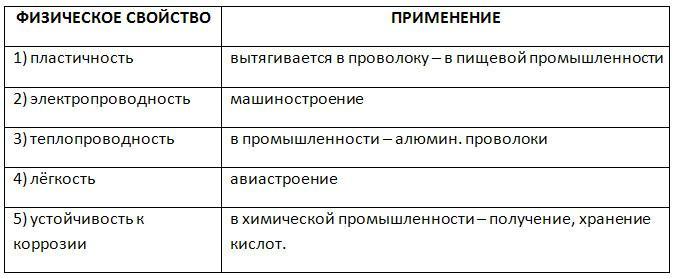
Алуминиеви сплави
Физическите свойства на медта и алуминия са такива, че когато се добави известно количество мед към алуминиева сплав, нейната кристална решетка се огъва и силата на сплавта се увеличава. Ал се основава на това свойство на легиране на леки сплави за повишаване на тяхната якост и устойчивост на агресивни среди.
Обяснението на процеса на втвърдяване е в поведението на медните атоми в кристалната решетка на алуминия. Cu частиците са склонни да изпадат от кристалната решетка на Al, групирани са в нейните специални области. 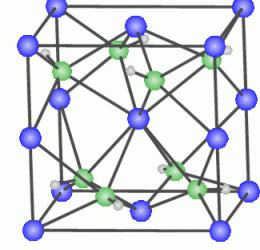 Когато медните атоми образуват клъстери, се образува смесена CuAl2 кристална решетка, в която сребърните метални частици се включват едновременно в общата кристална решетка от алуминий и в смесена CuAl2 решетка. в обикновеното. Това означава, че силата на новообразуваното вещество е много по-висока.
Когато медните атоми образуват клъстери, се образува смесена CuAl2 кристална решетка, в която сребърните метални частици се включват едновременно в общата кристална решетка от алуминий и в смесена CuAl2 решетка. в обикновеното. Това означава, че силата на новообразуваното вещество е много по-висока.
Химични свойства
Взаимодействието на алуминий с разредена сярна киселина и. T солна киселина. При нагряване този метал лесно се разтваря в тях. Студено концентрирано или силно разредено азотна киселина не разтваря този елемент. Водните разтвори на алкали активно влияят на веществото, в хода на образуването на алуминати - соли, които съдържат алуминиеви йони. Например:
Al2O3 + 3H2O + 2NaOH = 2Na [Al (OH) 4 ]
Полученото съединение се нарича натриев тетрахидроксалуминат.
Тънък филм на повърхността на алуминиевите изделия предпазва този метал не само от въздуха, но и от водата. Ако тази тънка бариера бъде премахната, елементът ще взаимодейства енергично с вода, освобождавайки водород от него.
2AL + 6H2O = 2 AL (OH) 3 + 3H2
Образуваното вещество се нарича алуминиев хидроксид.
AL (OH) 3 реагира с алкали за образуване на хидроксиалуминатни кристали:
Al (OH) 2 + NaOH = 2Na [Al (OH) 4 ]
Ако това химическо уравнение се добави към предишното, получаваме формулата за разтваряне на елемент в алкален разтвор.
Al (OH) 3 + 2NaOH + 6H2O = 2Na [Al (OH) 4 ] + 3H 2
Изгаряне на алуминий
Физическите свойства на алуминия позволяват да реагира с кислорода. Ако прахът от това метално или алуминиево фолио се нагрява, той мига и изгаря с бял ослепителен пламък. В края на реакцията се образува алуминиев оксид Al2O3 .
алуминий
Полученият алуминиев оксид има геоложкото име на алуминий. При естествени условия се среща под формата на корунд - твърди прозрачни кристали. Корундът се отличава с висока твърдост, индексът му в скалата на твърдите вещества е 9. Самият корунд е безцветен, но различни примеси могат да го оцветят в червено и синьо, така че се получават камъни, които в бижутата се наричат рубини и сапфири.
Физическите свойства на алуминиевия оксид позволяват отглеждането на тези скъпоценни камъни в изкуствени условия. Техническите скъпоценни камъни се използват не само за бижута, те се използват в прецизното изработване на инструменти, за направата на часовници и други неща. Изкуствени рубинови кристали също са широко използвани в лазерните устройства. 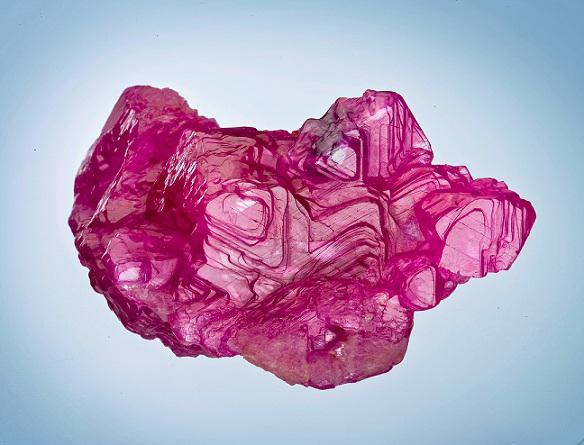
Дребнозърнести сортове корунд с голямо количество примеси, отлагани на специална повърхност, познати на всички като емери. Физическите свойства на алуминиевия оксид обясняват високите абразивни свойства на корунда, както и неговата твърдост и устойчивост на триене.
Алуминиев хидроксид
А1 (ОН) 3 е типичен амфотерен хидроксид. В комбинация с киселина, това вещество образува сол, съдържаща положително заредени алуминиеви йони, в алкали образува алуминати. Амфотерното вещество се проявява във факта, че може да се държи както като киселина, така и като алкална. Това съединение може да съществува в желеобразна или твърда форма.  Практически неразтворим във вода, но реагира с повечето активни киселини и основи. Физическите свойства на алуминиевия хидроксид се използват в медицината, той е популярен и безопасен начин за намаляване на киселинността в организма, използва се при гастрит, дуоденит, язви. В промишлеността като адсорбент се използва Al 2 (OH) 3 , той перфектно пречиства водата и утаява разтворените в него вредни елементи.
Практически неразтворим във вода, но реагира с повечето активни киселини и основи. Физическите свойства на алуминиевия хидроксид се използват в медицината, той е популярен и безопасен начин за намаляване на киселинността в организма, използва се при гастрит, дуоденит, язви. В промишлеността като адсорбент се използва Al 2 (OH) 3 , той перфектно пречиства водата и утаява разтворените в него вредни елементи.
Промишлена употреба
Алуминият е открит през 1825 година. Първоначално този метал се оценяваше над златото и среброто. Това се дължи на сложността на извличането му от руда. Физическите свойства на алуминия и способността му бързо да образува защитен филм на повърхността му затруднява изучаването на този елемент. Едва в края на 19-ти век е бил удобен метод за топене на чист елемент, подходящ за използване в промишлен мащаб. 
Лекотата и способността да се противопоставят на корозията са уникалните физични свойства на алуминия. Сплавите от този сребърен метал се използват в ракетната технология, в производството на автомобили, кораби, самолети и инструменти, в производството на прибори за хранене и прибори за хранене.
Като чист метал Al се използва при производството на части за химическо оборудване, електрически проводници и кондензатори. Физическите свойства на алуминия са такива, че неговата електрическа проводимост не е толкова висока, колкото тази на медта, но този недостатък се компенсира от лекотата на въпросния метал, което прави възможно да се направят телове от по-дебел алуминий. Така че, с една и съща електрическа проводимост, алуминиевата тел тежи два пъти по-малко от медта.
Също толкова важно е използването на Al в процеса на алуминизация. Това е така наречената реакция на насищане на повърхността на чугунен или стоманен продукт с алуминий, за да се предпази основният метал от корозия при нагряване.
В момента доказаните запаси от алуминиеви руди са доста сравними с нуждите на хората в този сребърен метал. Физическите свойства на алуминия могат да представят много повече изненади на изследователите си, а обхватът на приложение на този метал е много по-широк, отколкото може да се предположи.